023-67630383
 销售咨询QQ2548969917
销售咨询QQ2548969917 技术咨询QQ1291769782
技术咨询QQ1291769782热线/微信:13681365274
 销售咨询QQ2548969917
销售咨询QQ2548969917 技术咨询QQ1291769782
技术咨询QQ1291769782微信扫一扫
下载说明书


摘要
通过对包含在基因组DNA中的信息的差异时空访问,能够从单个基因组在多细胞生物中形成高度特化的细胞和组织并发挥其功能。表观基因组在如何获取DNA信息方面起着至关重要的作用,在过去的十年中,表观遗传异常和病理学之间的联系变得越来越清楚。因此,精确修饰表观基因组的方法作为潜在的新疗法引起了人们的兴趣。我们最近描述了一个平台,designer表观基因组修饰器(DEM),能够精确编辑细胞的表观基因组,以控制选定基因的表达。在这里,我们提供了一个详细的方案来简化鉴定有效地和选择性地结合到它们预期的靶位点并使靶基因的表达失活的DEMs的过程。此外,我们描述了以多重方式同时调节多达三个基因表达的程序。该方案分为四个阶段,指导用户完成多色报告细胞系的产生及其用于选择功能性DEM。所描述的整个过程的持续时间从使用单一报道基因时的约6周到使用三个报道基因微调所选DEMs的多重表观基因组编辑能力的13周不等。鉴于在生物医学研究的各个领域对表观基因组编辑的巨大兴趣,该协议将帮助科学家探索这些用于他们研究的新技术。

介绍
在生理条件下,细胞基因组中包含的信息只有一部分在特定时间是可获得的,这确保了只有编码特定细胞类型所必需的基因的基因组部分是活性的。这是通过能够以组织特异性方式直接影响基因表达的反式和顺式调节元件(CisE)的协同作用而成为可能的。一方面转录因子的活性和另一方面DNA或组蛋白的可遗传化学修饰有助于形成活生物体的许多不同细胞类型的同一性,这些细胞类型除了它们独特的功能之外,还共享相同的基因组。“表观基因组”是调节染色质结构的DNA和组蛋白修饰的集合。这个“代码”的解释是通过能够识别这些表观遗传标记并激活特定转录结果的特殊酶(即表观遗传读码器)的活性来保证的。表观基因组的维持由不同种类的酶控制,这些酶能够沉积或去除表观遗传标记(即,分别为表观遗传书写者和清除者)。这些特殊蛋白质的协同作用决定了细胞基因组中包含的信息在时间和空间上的不同存取方式。
以全基因组方式研究DNA和组蛋白修饰的新工具和技术的发展,显著增强了我们对表观遗传密码影响基因表达的机制的了解1。这突出了表观基因组的异常在包括自身免疫2、免疫3和癌症4在内的主要人类疾病中起着重要作用。因此,表观基因组本身已经成为一个潜在的治疗靶点,因为表观遗传标记具有一定的可塑性,可以用来恢复正确的基因调控。虽然外部刺激,如体力活动、营养和锻炼,会影响表观基因组,从而在治疗环境中起支持作用5,但在临床上也已经开发了能够通过干扰书写和擦除器的正常功能来改变整体表观基因组的化合物,即所谓的表位药物,以治疗某些形式的癌症6。然而,它们缺乏选择性是一个主要障碍,因为从不同的基因组背景(即启动子或基因体)添加或去除某种表观遗传标记,如DNA甲基化,可能对基因表达产生相反的结果7。类似地,抑制组蛋白乙酰化清除剂,如组蛋白脱乙酰酶3,既可以通过抑制巨噬细胞来改善动脉粥样硬化的发展,也可以导致内皮细胞死亡8,9。因此,开发工具和方法来有针对性地改变表观基因组是至关重要的。
几个工具,利用不同的策略,以一种简单明了的方式实现目标表观基因组编辑,现在是可用的10。在大多数情况下,这些系统已经在使用通常不适用于临床相关原代细胞的递送方法的细胞系中得到验证。为了克服这一技术限制,我们最近开发了一个平台,用于在原代人类T淋巴细胞中实现精确的表观基因组编辑11。我们设计的表观基因组修饰物(DEM)由来自黄单胞菌转录激活因子样效应子(TALE)的高度特异性DNA结合结构域组成,它定义了每个DEM的基因组靶位点。这融合到Krüppel相关盒(KRAB),人从头DNA甲基转移酶3A (DNMT3A)和鼠调节因子DNA甲基转移酶3样的C-末端结构域。在与预期的基因组靶位点结合后,每个DEM沉积DNA甲基化和组蛋白3赖氨酸9三甲基化,分别是DNMT3A和KRAB活性的结果。这些抑制性表观遗传标记的沉积导致异染色质的定向形成,随后靶基因沉默11。使用单个体外转录的mRNA可以将单个DEM递送到高度敏感的原代人类细胞中,并且可以利用该DEM通过表观基因组的基因座特异性改变来控制靶基因表达,从而补充了可用于以靶向方式控制基因表达模式的工具集。有了进行表观基因组编辑的分子工具,就有必要开发报道系统,使其能够容易地筛选特定应用的功能性DEM。此外,考虑到表观基因组编辑提供的以安全的方式同时改变多个基因表达的可能性7,需要有一个多重报告系统,该系统允许微调多个表观基因组编辑的同时递送,以说明多种多样的效应。
这里我们描述了如何建立一个基于多个荧光报告基因同时表达的系统。该系统为研究人员提供了使用流式细胞术进行小规模功能表观基因组编辑(如DEMs)筛选所必需的知识。重要的是,考虑到靶向不同序列的表观基因组编辑器的相对功效,该系统允许微调条件以同时实现多达三个基因的高效多重表观基因组编辑。所描述的报道系统不依赖于感兴趣基因的转录状态,因此允许用户在同一细胞系中选择针对任何感兴趣序列的最有效的表观基因组编辑器。与其他策略(如直接靶向内源性CisE)相比,该方案提供了用一个细胞系统(即HEK293T细胞)选择靶向任何感兴趣CisE的功能性表观基因组编辑的机会,而不依赖于其调节活性,也不考虑靶基因的表达水平。这一特点,结合完善的操作报告细胞的方案,使得该程序易于移植到任何实验室。值得注意的是,该系统代表了以前发表的单色报告基因的改进11,以前发表的单色报告基因仅限于筛选针对单一调节元件的功能性DEMs。
该方法的应用
近几十年来,表观遗传修饰和转录调控之间的联系已被进一步阐明,越来越多的证据表明,异常的表观基因组可能在疾病的易感性、表现和进展中发挥重要作用。然而,对于建立因果关系至关重要的表观遗传标记的定向操作技术,直到最近才被引入。与基因组编辑相比,靶向表观基因组编辑可以在不改变潜在基因组序列的情况下控制基因表达。因此,不同性质(即激活性或抑制性)的表观遗传标记的沉积可以以多重方式在不同的基因组位置同时进行,而没有多重基因组编辑时可能发生的有害基因组重排的风险12。为了通过表观基因组编辑改变基因表达,重要的是要有可用的表观遗传效应子,其能够高效地在靶位点沉积所需的表观遗传标记。在这种情况下,在确定了控制靶基因表达的CisE后,研究人员通常设计一系列效应子,经过繁琐的筛选程序,从中选择表现最佳的一个(或多个)用于进一步的实验。这一过程可能受到以下因素的阻碍:( I)进行筛选的细胞系统,因为它需要靶基因被转录或沉默,这取决于是否筛选转录阻遏物或激活物,和(ii)所用细胞系的有效转染方案的可用性。当用户的目的是同时控制多个基因的表达水平时,由于需要筛选多个效应物阵列以在所有靶基因座获得期望的结果,该过程变得更加复杂。这一方面是至关重要的,因为当一个效应子单独使用时可能是有效的,但由于对沉积表观遗传标记的宿主因子的竞争,它的效力可能在多重情况下受到影响。本文所述的方法允许以直接的方式同时筛选多组表观基因组编辑器(靶向多达三种不同的ci ),以选择用于下游表观基因组编辑应用的效应器的最佳表现组合。基于我们在使用该系统中获得的专业知识11,13,我们预计检索到的信息可用于指导更多相关细胞系的后续实验,并最终用于原代人类细胞。通过应用该方案,用户可以选择能够结合到其预期靶位点的效应物,并且可能能够在其天然环境中在所选CisE上沉积期望的表观遗传标记。该方案中描述的用于递送所选效应物的方法通常适用于更敏感的细胞,例如初级造血细胞11,14。最近描述的病毒系统对DEMs15进行矢量化的可用性为用户提供了在各种细胞系统中解决引人注目的科学问题所需的所有工具。
与其他方法的比较
虽然已经开发了多种平台来有效地修饰细胞的表观基因组,但是以并列方式评估表观基因组编辑器的功效以在可用阵列中选择最佳表现的方法是有限的。通常,研究人员依靠表达不同效应子的质粒同时转染多个细胞系来选择最有活性的一个16。在这种情况下,调节基因表达的失败可能是由于无效结合或局部染色质构象导致效应物的排斥,这些效应物可能在最终感兴趣的初级细胞系统中仍有功能。此外,由于缺乏有效转染所选细胞的既定方案,寻找最合适的细胞系来筛选表观基因组编辑活性可能会变得复杂。因此,用户需要多种替代细胞系来为进一步的实验确定最有效的效应器。我们的系统简化了筛选过程,因为它允许用户产生单个报告细胞系,该细胞系可用于鉴定功能性表观基因组编辑,而不管靶基因的内源表达水平。在这种情况下,选择完全基于效应子的结合能力,从而允许那些不能结合其预期靶位点的效应子被丢弃。这意味着当用于改变天然染色质环境中的CisE时,选择的效应子可能不起作用,我们通常建议选择两到三个表现最好的效应子进行后续验证。然而,根据我们的经验,按照我们的程序选择的高活性效应子通常也能够在其天然染色质环境中发挥作用,而不需要在其他替代细胞系中进行中间验证实验11。这允许用户在最终选择的细胞类型中或在原代人类细胞中直接使用所选择的效应子7。由于我们的方法依赖于常用的细胞系(HEK293T ),因此很容易获得成熟的递送方案,从而减少实验差异,并使该程序易于移植到任何实验室。此外,该平台的灵活性允许根据TALEs的DNA结合结构域或CRISPR–Cas靶向系统筛选各种表观遗传和转录修饰物(激活物和阻遏物)。重要的是,当以多重表观基因组编辑为目标时,效应子可能竞争相同的宿主细胞因子来沉积表观遗传标记,如果效应子没有被同时筛选,则导致不可预测的结果。
限制
筛选程序基于基于荧光的报道基因分析,其中三种不同的报道基因构建体中包含多达三种CisE,用于产生稳定表达三种荧光报道基因的细胞系。如果所有三种报告基因都是必需的,那么报告基因构建体和报告基因细胞系的产生都是耗时的,并且用户必须考虑在实验室中是否有合适的方法和专业知识,以及是否可以安全地使用特定的设备。重要的是,不同荧光团的重叠信号将兼容性限制为最多三个,以避免使用可能不总是可用的高度复杂的流式细胞仪。此外,我们的系统依赖于整合的报道基因构建体,其结果没有考虑到染色质结构,而染色质结构可能会影响其内源背景下的靶位点。为了增加内源性位点表观基因组编辑成功的可能性,我们建议使用我们的报告系统,并从每个初始阵列中选择两个或三个效应子来靶向单个CisE。尽管该方案可用于测试不同性质的表观基因组编辑的活性,但我们提供了筛选我们实验室先前描述的功能性DEM的细节11。用户应提前访问针对所选CisE的所需表观基因组编辑平台。我们建议使用易于组装的DEM,或者使用Addgene中可用的试剂盒,或者遵循我们之前公布的详细方案15。作为替代方案,靶向所需基因组位点的DEMs可以通过合作协议从该方案的作者处获得。
试验设计
在这里,我们描述了一个报告系统,它可以很容易地从三组针对不同ci的DEM中选择表现最好的表观基因组编辑器。当同时递送DEM时,即当多路复用时,该系统揭示了效应器相对效率的差异,并可用于微调条件以实现多路复用方式的高效表观基因组编辑。整个过程如图1所示,可分为四个阶段。首先,用户需要定义将要进行表观基因组编辑的CisE。这可以是,例如,控制给定靶基因表达的已知启动子或增强子序列,或以用户想要剖析的难以捉摸的调控网络为特征的CisE。在CisE中,考虑到每个DEM与单个基因组序列结合,用户必须定义所需数量的靶位点。我们建议在每个选择的CisE中选择6到10个目标站点,并确保访问相应的DEM阵列,如前一节所述。为了最大化靶向效率,重要的是考虑位于开放染色质区域的靶位点,如所述11,17。一旦确定了选择的CisE,用户必须创建荧光报告基因,每个荧光报告基因包含一个位于荧光报告基因表达盒上游的CisE(阶段1)。我们的系统经过优化,最多可结合三种不同的荧光报告基因,因此一次最多可包含三种不同的CisE。这也允许使用单一系统,通过同时递送靶向不同ci的效应子,在多重设置中测量表观基因组编辑的效率。随后,使用整合病毒载体将报道构建体整合到HEK293T细胞的基因组中,以产生多色报道细胞系(阶段2)。我们描述了通过三种病毒载体的系列转导产生多色报告细胞系的程序。这降低了由于报道基因的瞬时表达(即假转导)而导致的可变性,并控制了载体整合拷贝的数量。此外,具有稳定表达报道基因构建体的细胞系允许评估由于在靶CisE位点进行表观基因组编辑而产生的长期效应。原则上,这三种病毒可以组合成一个单一的转导事件,然后对表达这三种报道基因的细胞进行单细胞分选。尽管对该方案的这种修改可能有助于减少产生多色报道细胞系所需的时间,但它可能导致分离出具有每个载体的多个整合拷贝的克隆,因为在这种情况下每个载体具有单一整合拷贝的可能性非常低,如参考文献1所述。18.因此,我们建议进行连续转导,除非是绝对必要的。有了针对每个选择的CisE的表观基因组编辑器的可用阵列,用户可以使用阶段2中产生的报告细胞系来从每个阵列(阶段3)中鉴定表现最佳的效应子。随后,通过确定实现有效表观基因组编辑所需的最小剂量,根据它们的效力来表征所选择的DEM,并且最终可以在多重设置中验证结果,以在所有测试的CisE中实现具有相似效力的有效表观基因组编辑(阶段4)。重要的是,阶段2中产生的多色细胞系不同于我们以前报道的单色系统,11因为它同时表达两种额外的荧光报告基因,每种都含有不同的CisE。数据分析部分已相应扩展,以适应这一改进,这是以多路方式筛选功能性DEM所必需的。将DEM递送到多色报告细胞的下游程序与之前描述的11,14相同,但增加了同时递送最多三个DEM的细节,每个DEM靶向不同的感兴趣的ci。
图1:实验工作流程的概述。
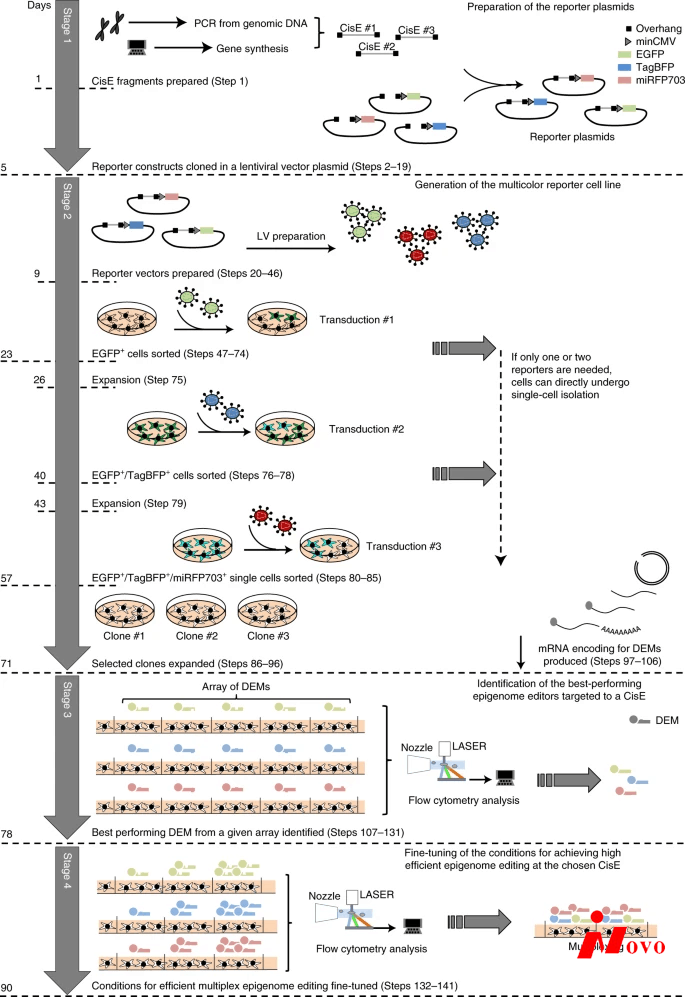
从基因组DNA中分离或化学合成多达三种选择的CisE,并包括在所述的报道质粒中。在慢病毒(LV)载体产生后,重组病毒用于产生所需的报道细胞系。用户可以分离含有一个、两个或三个整合报道基因的单细胞,然后用它们来筛选靶向所选CisE的表观基因组修饰物阵列。报告细胞也可用于微调条件,以在选择的CisE下使用所选的最佳表现表观基因组修饰物实现高效的多重表观基因组编辑。
https://www.nature.com/articles/s41596-020-0380-y